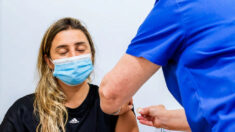
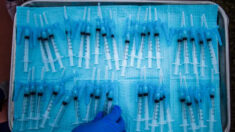
Na sexta-feira (08), a Food and Drug Administration (FDA) dos EUA aprovou a tecnologia CRISPR e terapias genéticas baseadas em vetores lentivirais para o tratamento da doença falciforme em pacientes com 12 anos ou mais.
“As ações de hoje seguem avaliações rigorosas dos dados científicos e clínicos necessários para apoiar a aprovação”, disse o Dr. Peter Marks, diretor do Centro de Avaliação e Pesquisa Biológica da FDA.
As duas terapias são Casgevy, uma terapia genética baseada em CRISPR fabricada pela Vertex, e Lyfgenia da Bluebird Bio, que não usa CRISPR, mas vetores lentivirais para editar genes.
Os resultados dos ensaios clínicos mostraram que ambos os tratamentos podem reduzir a dor causada por eventos vaso-oclusivos, características da doença falciforme.
Eventos vaso-oclusivos são casos em que os vasos sanguíneos ficam bloqueados, o que pode causar danos aos órgãos e dor intensa.
“Sabemos que eles transformam a vida das pessoas; eles erradicam significativamente – se não completamente – e eliminam esses eventos horríveis e dolorosos que tomam conta da vida das pessoas com células falciformes… O que não sabemos é o que acontece com o funcionamento dos órgãos”, Dra. Julie Kanter, codiretora do Lifespan Comprehensive Sickle Cell Center da Universidade do Alabama, disse em uma entrevista com a universidade.
Qual é a doença da célula falciforme?
A doença falciforme é uma doença hereditária do sangue.
Mutações em um gene da hemoglobina fazem com que o corpo forme hemoglobina deformada, proteínas nos glóbulos vermelhos responsáveis pelo transporte de oxigênio.
Quando a hemoglobina é deformada, torna-se mais pegajosa e incapaz de transportar oxigênio. Além disso, os glóbulos vermelhos ficam deformados, formando uma forma crescente ou de “foice”.
“Então, normalmente, os glóbulos vermelhos não são pegajosos. Eles fluem facilmente pelos vasos sanguíneos como a água pelos canos. Mas em pessoas com doença falciforme, nos minúsculos canos, eles podem ficar presos”, disse o Dr. Kanter na entrevista.
“Essa é uma das principais razões pelas quais as pessoas acabam tendo dor ou danos aos órgãos associados à doença falciforme.”
Pessoas com doença falciforme herdaram a mutação em ambos os genes. Em média, vivem até 52 anos, sendo esse tempo marcado por anemia, episódios de dor, infecções, transfusões de sangue e muito mais.
Os transplantes de células-tronco de um doador trataram com sucesso a doença falciforme em crianças, com alguns estudos relatando uma taxa de sucesso superior a 80%. A operação é muito mais arriscada à medida que o paciente envelhece.
Terapias genéticas: novas opções de tratamento
Atualmente, existem opções limitadas de tratamento para pacientes com doença falciforme que gostariam de ser curados da doença, especialmente se não tiverem um irmão compatível que possa doar suas células-tronco ao paciente.
Casgevy e Lyfgenia são terapias autólogas e usam células extraídas do paciente que recebe o tratamento, “portanto, os pacientes não precisam de um doador. Teoricamente, todos podem ser seus próprios doadores”, Akshay Sharma, médico-cientista do Departamento de Transplante de Medula Óssea e Terapia Celular do St. Jude Children’s Research Hospital, escreveu ao Epoch Times por e-mail.
As terapias genéticas recentemente aprovadas visam corrigir a mutação, substituindo o gene defeituoso.
As células-tronco do sangue seriam colhidas, examinadas em busca de defeitos, editadas e devolvidas ao paciente.
Casgevy, usando a tecnologia CRISPR, poderia substituir a seção mutada nas células pelas sequências genéticas corretas. O outro tratamento, Lyfgenia, utiliza um vetor lentiviral para adicionar um bom gene de hemoglobina ao DNA celular de um paciente.
Antes do tratamento, os pacientes devem ser submetidos à quimioterapia para remover outras células-tronco da medula óssea e substituí-las pelas células modificadas. Todo o processo pode levar vários meses.
Dados que apoiam Casgevy e Lyfgenia
A eficácia e segurança do Casgevy foram avaliadas num ensaio em curso com 44 crianças e adultos. Os pacientes foram acompanhados por 24 meses e deveriam ter atingido pelo menos um ano sem crises vaso-oclusivas (COV) graves.
No momento da submissão à FDA, apenas 31 pacientes puderam ser avaliados. Após o tratamento, 29 deles ficaram livres de COV durante pelo menos um ano.
Os efeitos colaterais comuns entre os 44 participantes foram “níveis baixos de plaquetas e glóbulos brancos, feridas na boca, náuseas, dor musculoesquelética, dor abdominal, vômitos, neutropenia febril (febre e baixa contagem de glóbulos brancos), dor de cabeça e coceira”, segundo ao comunicado de imprensa do FDA.
A Lyfgenia, por outro lado, foi avaliada ao longo de 24 meses em 32 pacientes. Vinte e oito, ou 88%, dos pacientes alcançaram uma resolução completa dos eventos vaso-oclusivos de seis a 18 meses após a infusão.
Lyfgenia compartilha efeitos colaterais semelhantes com Casgevy.
Sharma disse que seria mais cauteloso ao prescrever tratamento para seus pacientes pediátricos.
“Ambas as terapias foram aprovadas com base em um pequeno número de pacientes acompanhados por um período de tempo relativamente curto. Este é um acompanhamento muito limitado em uma população muito limitada de pacientes para uma terapia que altera a vida. Os resultados são impressionantes, procuro durabilidade e segurança a longo prazo – que estarão disponíveis com o tempo.”
Aviso de caixa preta para Lyfgenia
O ensaio para Casgevy está em andamento e os riscos a longo prazo são desconhecidos.
Entretanto, o ensaio Lyfgenia detectou dois casos de câncer no sangue entre sete pacientes. A empresa inicialmente interrompeu o estudo em fevereiro de 2021, mas o retomou após concluir que era improvável que o caso de câncer mais recente estivesse relacionado à terapia genética.
No entanto, “uma caixa preta está incluída no rótulo do Lyfgenia com informações sobre este risco. Os pacientes que recebem este produto devem ter monitoramento vitalício para essas doenças malignas”, escreveu o FDA.
Tecnologia CRISPR sugestiva para riscos de câncer
Também existem preocupações sobre a terapia genética CRISPR.
Estudos de 2022 sobre tecnologia CRISPR mostraram que a tecnologia pode causar grandes rearranjos do DNA através de um processo chamado retrotransposição, conhecido por desencadear o câncer.
Os eventos de retrotransposição causados pelo CRISPR ocorrem de 5% a 6% das vezes, de acordo com um comunicado de imprensa sobre o estudo. Os autores não estudaram esta tecnologia em células estaminais do sangue, mas sim em células embrionárias e cancerígenas humanas em laboratório, pelo que não se sabe se os mesmos efeitos podem ser observados em ambientes do mundo real.
“Precisamos determinar com que frequência a retrotransposição ocorre em ensaios clínicos de terapias genéticas CRISPR”, disse o autor do estudo, Dr. Robert Chiarle, em um comunicado à mídia.